界面新聞記者 |陳楊
界面新聞編輯 |謝欣
8月26日盤后,創(chuàng)新藥明星公司康方生物發(fā)布2025年上半年業(yè)績。當期,公司營收14.12億元,同比增長37.75%,其中商業(yè)銷售收入14.02億元,同比增長49.20%;虧損5.88億元,較上年同期虧損2.49億元有所增加。
公司稱,商業(yè)銷售收入增長主要源于卡度尼利單抗(AK104,PD–1/CTLA–4雙抗)、依沃西單抗(AK112,PD–1/VEGF雙抗)自今年1月起納入國家醫(yī)保后帶來的銷售量增長。
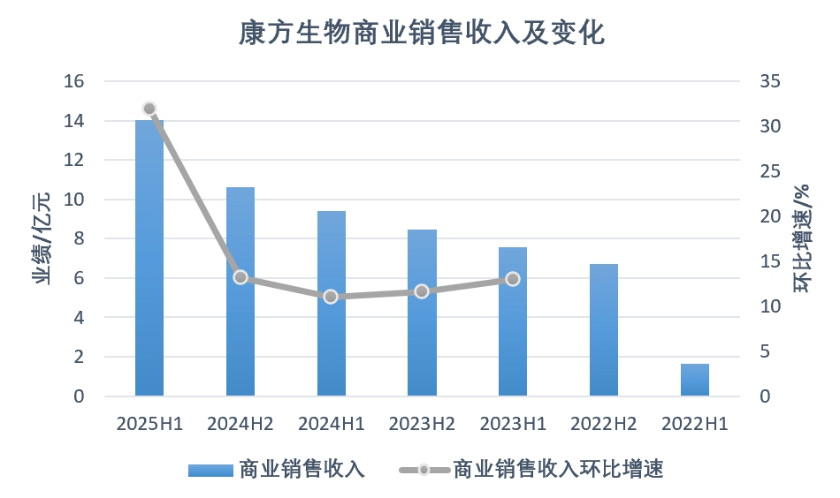 數據來源:康方生物年報、演示材料。界面新聞記者陳楊制圖
數據來源:康方生物年報、演示材料。界面新聞記者陳楊制圖
同期,公司虧損金額增長的原因則包括參股合作方美股上市公司Summit而計提的股權投資損失由去年同期的3260萬元增加至1.92億元;研發(fā)投入由5.94億元增至7.31億元;以及計提股權激勵費用由530萬元增長至2720萬元。
8月27日開盤,康方生物股價一路走低,收盤價報159港元/股,跌5.92%,當下市值1427億港元。
據界面新聞梳理,目前,康方生物共計獲批7款產品,除前述兩款核心雙抗,還包括派安普利單抗等三款合作開發(fā)或授權出去的PD-(L)1單抗,以及分別在2024年9月、今年5月獲批的伊努西單抗(PCSK9單抗)、依若奇單抗(IL-12/IL-23單抗)。后兩者將公司進入商業(yè)化階段的產品范圍由腫瘤擴大至代謝/自免領域。
康方生物亦提到,其銷售團隊由上年同期的800余人增至1200余人,覆蓋腫瘤和特藥兩大領域。界面新聞注意到,2024年,康方生物商業(yè)化團隊經歷調整。郭永接替石文俊成為新的商業(yè)化負責人,任首席商業(yè)官,前者此前在科倫博泰及多家跨國藥企任職。
不過當下,市場關注的焦點仍大多集中在AK112身上。
 AK112在肺癌領域的布局。界面新聞截自康方生物2025年中期業(yè)績演示材料
AK112在肺癌領域的布局。界面新聞截自康方生物2025年中期業(yè)績演示材料
康方生物在本次公告中披露,AK112在國內的III期臨床HARMONi-A研究中達到OS(總生存期)臨床終點,取得具有統(tǒng)計學顯著和臨床意義顯著的OS獲益。
界面新聞注意到,該研究的適應證為聯合化療治療EGFR-TKI治療后進展的非小細胞肺癌,這也是AK112在國內于2024年5月獲批的首個適應證。而此前,康方生物曾公布該研究的PFS(中位生存期)數據,還引起市場誤讀、股價大跌、公司緊急回應。
另外,HARMONi-A對應的全球III期臨床為HARMONi研究。今年5月,Summit亦公布了后者的頂線結果,這也是該藥的首個全球III期臨床數據讀出。其中,AK112在主要終點PFS上取得統(tǒng)計學顯著且具臨床意義的改善,風險比(HR)為0.52;在另一主要終點OS上則顯示出積極趨勢,但未達到統(tǒng)計學顯著獲益,風險比為0.79(p=0.057)。
Summit稱,基于HARMONi臨床試驗結果,其計劃提交生物制品許可申請(BLA),時間將基于與美國食藥監(jiān)局(FDA)的討論。
不過界面新聞了解到,EGFR-TKI治療后進展的非小細胞肺癌實際上是一個相對較小的適應證,年銷售額潛力約在5億至10億美元。相比之下,一線治療野生型非小細胞肺癌更是市場關注和AK112等產品追逐的“星辰大海”。
2024年5月,AK112正是在單藥一線治療PD-L1陽性非小細胞肺癌的國內注冊性III期臨床(HARMONi-2研究)中,在PFS上頭對頭戰(zhàn)勝了默沙東的PD-1帕博利珠單抗(俗稱“K藥”),顯示出取代K藥的潛力,因而一舉出圈,并掀起了一波PD-(L)1/VEGF雙抗交易潮,其中不乏今年輝瑞與三生制藥超60億美元的“天價”交易。
界面新聞注意到,到今年4月,AK112亦在國內獲批一線治療PD-L1陽性非小細胞肺癌適應證,同時公布的HARMONi-2研究初步OS數據也再次引發(fā)爭議。AK112在國內外醫(yī)療實踐下是否能得到具有統(tǒng)計學意義的OS數據成為市場關注的焦點。
目前,HARMONi-2研究對應的全球III期臨床HARMONi-7正在入組中,后者針對一線治療PD-L1 TPS≥50%的非小細胞肺癌。界面新聞在此前的公司業(yè)務溝通會上獲悉,康方生物創(chuàng)始人、董事長夏瑜曾表示,以現有的數據看對Summit在HARMONi-7研究上能取得成功非常有信心。
另在國內,AK112在HARMONi-6研究中頭對頭戰(zhàn)勝了百濟神州的替雷利珠單抗,由此遞交的第三個適應證上市申請已獲國家藥監(jiān)局受理,即與化療聯用一線治療鱗狀非小細胞肺癌。
不過隨著默沙東、輝瑞、BMS等大廠都手握同靶點產品,誰將買下Summit或是最大懸念。今年7月初有市場聲音指向同為跨國藥企的阿斯利康,但該消息未被后者證實。
除AK112外,AK104也已在國內獲批三項適應證,覆蓋宮頸癌全線和胃癌一線治療。另外,公司還啟動了該藥聯合侖伐替尼治療二線肝癌的全球多中心注冊性II期臨床。
手握兩款核心雙抗,康方生物在今年上半年提出了“IO(腫瘤免疫)2.0+ADC(抗體偶聯藥物)2.0”策略。
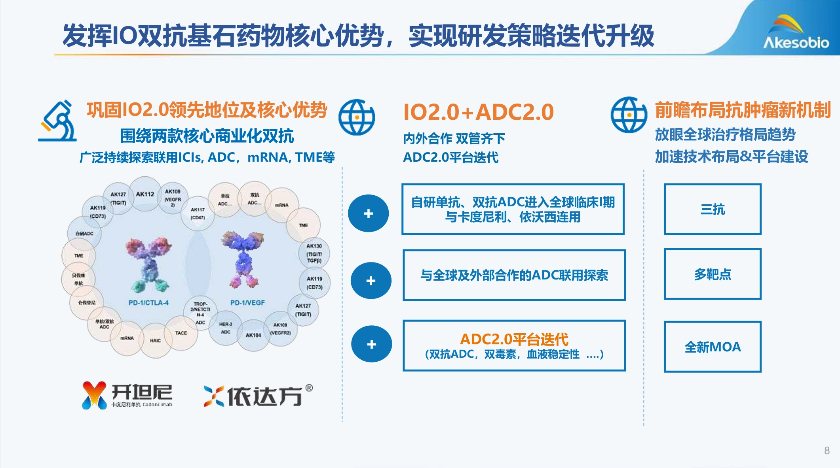 康方生物“IO2.0+ADC2.0”研發(fā)策略。界面新聞截自康方生物2025年中期業(yè)績演示材料
康方生物“IO2.0+ADC2.0”研發(fā)策略。界面新聞截自康方生物2025年中期業(yè)績演示材料
2023年,美國食藥監(jiān)局批準Padcev(Nectin4 ADC)與K藥聯用治療尿路上皮癌,由此腫瘤治療進入“IO+ADC”時代,這也是前幾年ADC領域交易十分火熱的原因。一年后,AK112“走紅”,PD-1/VEGF雙抗作為PD-1單抗的“升級版”,拉開“IO2.0+ADC”序幕,但目前還沒有這類聯用療法獲批。
8月27日,界面新聞從康方生物業(yè)績說明會上獲悉,夏瑜提到,公司從2012年成立開始做雙抗,當年雙抗的開發(fā)如火如荼,但直到今天能夠做到POC(概念驗證)的實際上沒有這么多。原因之一在于平臺結構,這將影響到最終能否成藥。
她戲稱,“就像不是所有牛奶都是特侖蘇,不是所有PD-1/VEGF都是依沃西”,一定要最終得到真正的臨床驗證。在她看來,AK112和AK104已不僅在在研階段,而是在商業(yè)化上已經成熟的雙抗。這兩個IO2.0雙抗作為基石性藥物,與ADC、小分子等聯用都具有優(yōu)勢,是公司研發(fā)策略迭代的重要一點。
ADC2.0則指雙抗ADC、雙毒素、優(yōu)化血液穩(wěn)定性等方向,是ADC藥物的“進化體”。康方生物自研的AK138D1(HER3 ADC)、AK146D1(Trop2/Nectin4 ADC)均處于臨床I期。
界面新聞注意到,康方生物也并非唯一提出相關策略的公司。在今年的研發(fā)日上,信達生物亦提出”IO+ADC的雙重升級”策略,其ADC的升級方面和康方生物類似,IO方面則已有PD-1/IL-2α-bias雙抗融合蛋白等在研產品冒頭,獲批開展全球關鍵III期臨床。這其中既可見國內頭部公司近幾年搭建、優(yōu)化技術平臺、自身積累起豐富的管線組合;亦可見腫瘤領域產品競爭之激烈、迭代速度之快。
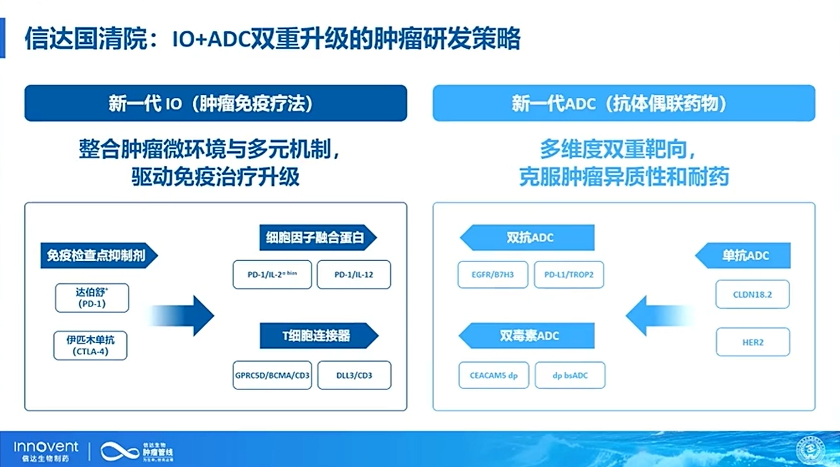 信達生物“IO+ADC”雙重升級研發(fā)策略。界面新聞截自信達生物2025年研發(fā)日演示材料
信達生物“IO+ADC”雙重升級研發(fā)策略。界面新聞截自信達生物2025年研發(fā)日演示材料
后續(xù)管線上,康方生物的古莫奇單抗(IL-17單抗)上市申請已獲國家藥監(jiān)局受理;曼多奇單抗(IL-4Rα單抗)中重度特應性皮炎III期注冊臨床達到研究終點,界面新聞獲悉其將在2026年上半年遞交國內上市申請。截至2025年上半年末,康方生物現金及等價物、其他短期金融資產總計71.38億元。

 京公網安備 11010802028547號
京公網安備 11010802028547號